【物理】
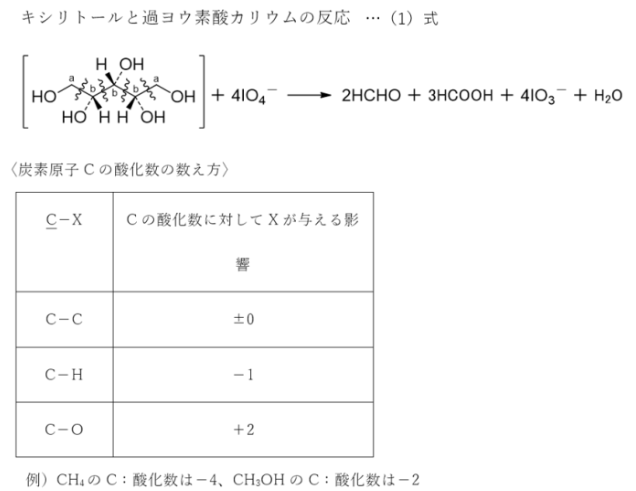
キシリトールと過ヨウ素酸カリウムの反応を以下に記載する。...(1)式とする。
1 誤。キシリトールC5H12O5と過ヨウ素酸カリウムKIO4との反応で酸化数が変化している原子は、炭素Cとヨウ素Iである。
(1)酸素Oについて
キシリトール中のOの酸化数は-2であり、反応後もOの酸化数は-2である。
(2)炭素Cについて
キシリトール中のaにおけるCの酸化数は-1であり、bにおけるCの酸化数は0であるが、酸化反応後、生成するホルムアルデヒドHCHOにおけるCの酸化数は0であり、ギ酸HCOOHにおけるCの酸化数は+2である。
(3)ヨウ素Iについて
IO4-におけるIの酸化数は+7であるが、反応後のIO3-におけるIの酸化数は+5である。
2 誤。( A )は、チオ硫酸ナトリウムである。本定量法は、キシリトールに過量の過ヨウ素酸カリウムKIO4を加え反応させた後、ヨウ化カリウムにより遊離させたヨウ素をチオ硫酸ナトリウムで滴定する。
3 正。( B )は、デンプン試液である。本定量法は酸化還元滴定であり、遊離したヨウ素をチオ硫酸ナトリウムで滴定するため、指示薬としてデンプン試薬を使用する(青色→無色)。
4 誤。1 molのキシリトールC5H12O5は、4 molの過ヨウ素酸カリウムIO4-によって酸化され、炭素-炭素結合が開裂し、2 molのホルムアルデヒドHCHOと3
molのギ酸HCOOHが生成される。よって、( C )はホルムアルデヒドHCHOである((1)式より)。炭素-炭素結合が開裂するため、アセトアルデヒドCH3CHOは生成されない。
5 正。( D )はギ酸HCOOHである((1)式より)。
